CO是常见的化学物质,在工业生产中用途很广泛.(1)已知:某些反应的热化学方程式如下:2H2(g)+SO2(g)=S(g)+2H2O(g)△H=+90.4kJ?mol-12CO(g)+O2(g)=2C
问题描述:
CO是常见的化学物质,在工业生产中用途很广泛.(1)已知:某些反应的热化学方程式如下:
2H2(g)+SO2(g)=S(g)+2H2O(g)△H=+90.4kJ?mol-1
2CO(g)+O2(g)=2CO2(g)△H=-556.0kJ?mol-1
2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ?mol-1
请写出用CO除去空气中SO2,生成S(g)及CO2热化学方程式___
(2)某燃料电池以CO为燃料,以空气为氧化剂,以熔融态的K2CO3为电解质,请写出该燃料电池正极的电极反应式___;
(3)在某温度下、容积均为2L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2H2(g)+CO(g)?CH3OH(g);△H=-dJ?mol-1(d>0).初始投料与各容器达到平衡时的有关数据如下:
| 实验 | 甲 | 乙 | 丙 |
| 初始投料 | 2molH2、1molCO | 1mol?CH3OH | 4molH2、2molCO |
| 平衡时n(CH3OH?) | 0.5mol | n2 | n3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 体系的压强 | P1 | P2 | P3 |
| 反应物的转化率 | α1 | α2 | α3 |
②三个容器中的反应分别达平衡时各组数据关系正确的是___(填序号).
A.α1+α2=1??B.Q1+Q2=dC.α3<α1???D.P3>2P1=2P2E.n2<n3<1.0mol?????F.Q3<2Q1
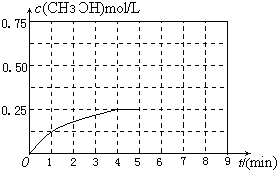
③在其他条件不变的情况下,将甲容器的体系体积压缩到1L,若在第8min达到新的平衡,从开始到新平衡时H2的转化率为65.5%,请在右图中画出第5min?到新平衡时CH3OH的物质的量浓度的变化曲线.
(4)实验室常用甲酸(一元酸)来制备CO.已知25℃时,0.l?mol/L甲酸(?HCOOH)溶液和0.l?mo1/L乙酸溶液的pH分别为2.3和2.9.现有相同物质的量浓度的下列四种溶液:①HCOONa溶液?②CH3COONa溶液③Na2CO3④NaHCO3溶液,其pH由大到小的顺序是___(填写溶液序号).关于0.l?mo1/L?HCOOH溶液和0.l?mo1/LHCOONa等体积混合后的溶液描述正确的是___.
a.c(HCOOˉ)>c(HCOOH)>c(Na+)>c(H+)
b.c(HCOOˉ)+c(HCOOH)=0.2mo1/L
c.c(HCOOˉ)+2c(OHˉ)=c(HCOOH)+2c(H+)
d.c(HCOOˉ)>c(Na+)>c(H+)>c(OHˉ)
 最佳答案:
最佳答案: (1)由①2H2(g)+SO2(g)=S(g)+2H2O(g)△H=+90.4kJ?mol-1②2CO(g)+O2(g)=2CO2(g)△H=-556.0kJ?mol-1③2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ?mol-1;根据盖斯定律反应①+②-③可得到2CO(g)+SO2...
版权声明
声明:有的资源均来自网络转载,版权归原作者所有,如有侵犯到您的权益
请联系本站我们将配合处理!
